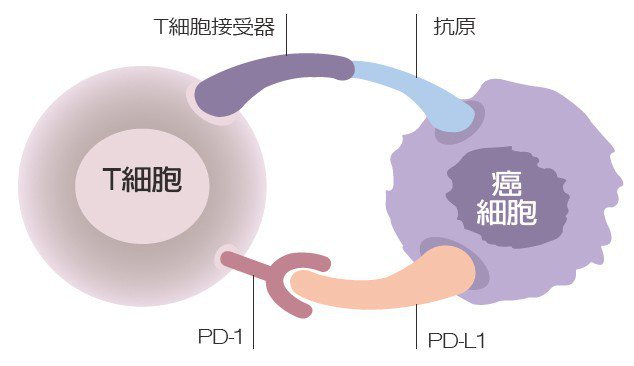
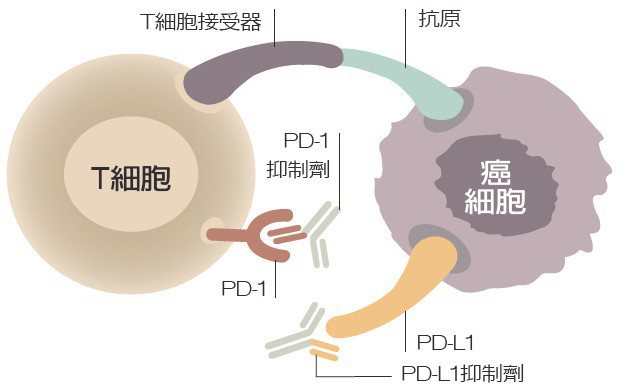
好萊塢知名女星安潔莉娜裘莉,因為母親過世於卵巢癌,阿姨過世於卵巢癌,接受基因檢測;並得知自己帶有BRCA1基因突變,已於2013年初接受預防性雙乳房切除手術,並考慮接著接受預防性雙側輸卵管及卵巢切除手術。消息傳出,引起國際輿論矚目,並登上時代雜誌封面頭條,更成為國內外醫學界的討論熱門話題之一。不過,真正值得普羅大眾深思的,則是,是否每個人都需要面對並做下安潔莉娜裘莉的抉擇?
大多數癌症為基因後天偶發突變發生,但是有一部分族群病人(約5-10%),是因為帶有先天germ line遺傳基因缺陷導致癌症發生。最著名的代表即為遺傳性乳癌與卵巢癌症候群(hereditary breast and ovary cancer syndrome),促成這個症候群最重要的兩個的基因是BRCA1與BRCA2。
遺傳基因與致癌機轉
BRCA1與BRCA2是1990年代在美國發現的。1990年,Hall等人研究早發與遺傳性乳癌家族,經由連鎖遺傳學定律(linkage analysis),發現染色體17q21與早發家族性乳癌有高度相關。其後1994年,Miki等人證染色體17q21上的BRCA1基因為造成乳癌(與卵巢癌)的基因。同年,Wooster等人發現位於13q12 -13也與乳癌發生相關,因而找到BRCA2基因。BRCA1有24個exon,轉譯而成的BRCA1蛋白質共有1863個胺基酸;BRCA2有27個exon,轉譯而成的BRCA2蛋白質共有3418個胺基酸。
BRCA1與BRCA2這兩個基因是屬於抑癌基因(tumor-suppressor gene),負責雙股DNA損壞的修復機轉。當細胞內雙股DNA損壞,細胞有兩個方式負責修補,第一個修復的方式稱為同源重組(homologous recombination),另一個是非同源染色體結合(non-Homologous end-joint),只有經由同源重組的方式來修復,雙股DNA才可以正確無誤的修復(圖2)。而BRCA1與BRCA2所參與的雙股DNA修復機轉,即是同源重組,因此,若這兩個基因其中之一發生缺陷,則雙股DNA受到攻擊斷裂後,會無法正確修復當細胞內DNA壞損累積到一定程度,則細胞就會發生癌變[2]。簡述其整個修復機轉,當細胞內雙股DNA損壞時,damage-response kinase ATM (ataxia–telangiectasia mutated) 與ATR (ataxia–telangiectasia and Rad3–related)就會被啟動,進而活化(磷酸化)BRCA1,使斷損的雙股DNA,進入同源重組 (homologous recombination) 的修復,有許多蛋白質參與其中,主要為Fanconi’s pathway相關蛋白質,BRCA2就是13個Fanconi’s pathway相關蛋白質中的FANCD1。若是在這個13個Fanconi’s pathway相關的對偶基因發生缺陷,會造成骨髓的Fanconi氏貧血、先天性疾病、白血病與癌症,當然也包含乳癌。
所謂遺傳性BRCA1與BRCA2帶因者,定義是來自父親或是母親的生殖細胞上(germline)帶有BRCA1或是BRCA2的基因突變,也就是說在一對染色體上,有其中一條染色體上的BRCA基因是有缺陷的(另一個是好的),當人體在生長過程中,因環境或是其他因素,另一條染色體上的BRCA1或是BRCA2 亦發生變異時,使BRCA1或是BRCA2的對偶基因完全喪失其功能,此時,容易發生乳癌(包括男性乳癌,BRCA2相關)、卵巢癌、胰臟癌與攝護腺癌等。因此,遺傳學家定義BRCA1與BRCA2帶因者為顯性遺傳,癌發的機率亦隨著年紀上升而累積;帶有 BRCA突變者,其乳癌等的發生年紀較一般病人早(20-30歲即開始有乳癌風險),終其一生發生乳癌的機率約到達40-87% (至70歲估計),卵巢癌的機率約到達16-60% (至70歲估計)。這兩個基因中,BRCA1又比BRCA2對乳癌有較重要的影響;若分開計算,則BRCA1帶因者終其一生乳癌發生機率為65-80%,卵巢癌為37-62%;BRCA2帶因者終其一生乳癌發生機率為45-85%,卵巢癌為11-23%。
基因突變的判讀
傳統認知上,一個抑癌基因發生突變,其抑癌(tumor suppression)功能可能就喪失,因此造成癌症發生。但是,BRCA1與BRCA2是相當大的蛋白質,某些情形下,若只是一個不影響功能的區域發生突變,則可能不影響其本身功能。在BRCA1與BRCA2上,當一個基因檢測,發現有基因突變時,需要小心的判讀,有的是良性的基因變異(benign polymorphism),與致癌無關;有的是致病性的突變(deleterious mutation)。然而,在BRCA1與BRCA2上,仍然有許多點突變位置,目前無法確定是良性或是致病性的基因變異,被歸類成未明確的變異(variants of uncertain significance,VUS)。舉例來說,當BRCA1發生C端(C-terminus)BRCT domain的刪除缺損(deletion)時,則BRCA1功能缺失,為致病性的突變;又如BRCA1發生M1775R的點突變時,也是致病性的突變;但是BRCA1發生S1613G的點突變時,則是良性的基因變異,與致癌無關。
BRCA基因突變相關的乳癌型態
BRCA1突變相關的乳癌以三陰性乳癌為主(estrogen receptor(-), progesterone receptor (-), Her2 (-)),但是隨著病患年紀的增長,三陰性乳癌的比例逐漸降低,取而代之的是estrogen receptor(+)乳癌。而BRCA2突變以賀爾蒙接受體陽性乳癌為主 ,但是隨著病患年紀的增長,三陰性乳癌的比例卻是逐漸上升。
亞洲國家與台灣資料
亞洲國家也針對此基因研究,證實BRCA1與BRCA2在早發乳癌占有一種要角色。於新加坡的研究中,收集了90個家族性或是早發乳癌病人 (小於35歲),經由分子生物學檢測與電腦計算,BRCA1與BRCA2的帶因者高達18.9 %。在另一個中國大陸的研究,收集了139位家族性或是早發乳癌病人,BRCA1的突變在家族性乳癌病人占了5.9 %而早發乳癌病人占了2.8 %。韓國也於2007年發表206位病人的研究,共有18.4 %病人發現了BRCA1與BRCA2的基因突變。東南亞國家(越南、菲律賓與馬來西亞)亦發表在家族性或是早發乳癌病人,4-10 %不等的BRCA1與BRCA2的突變機率。2009年,Hall教授等人,使用 Myraid資料庫分析BRCA1與BRCA2的突變機率與人種的差別,亞洲人種的突變基因機率與西歐婦女並沒有統計上的差異,其機率是相當的
台灣目前並沒有大規模研究資料,早年高雄醫學大學附設醫院與彰化基督教醫院曾做過小型研究。台大醫院張金堅教授(現任澄清醫院院長)與多位乳癌醫師於多年前開始研究此一基因對台灣病人的影響[14]。當時收案36個家族,針對家族有多位乳癌或是卵巢癌之病友或是早發之乳癌病友,徵得其同意之下,從事遺傳諮詢與基因診斷,以提供其風險評估。有4個家族(11%)被證實帶有BRCA1的germline突變。其中2個是遺傳密碼位移突變(frame-shift),1個是無義突變[non-sense mutation],另1個點突變。而這個點突變在當時國際上資料庫報告很少,分類上是屬於未明確的變異,該研究經由蛋白質結構分析與兩種功能性分析(transcription activation與yeast growth-inhibition assays),才推定該點突變應屬於致病性的突變,而該病人的乳癌病理組織也的確屬於三陰性乳癌,家族上也兩代多位成員發生乳癌。從該家族研究可以得知,台灣的確存在有BRCA1的家族。
何時建議進行基因檢測?
BRCA在媒體的報導之下,何時該檢測基因是大眾關心的議題。如同過往的研究,早發或是有家族史的乳癌病友,才會被建議進行基因檢測,由此可知,需要基因檢測的乳癌病友,是少數的族群。為了更精準的抓出BRCA基因突變的家族,有許多研究著墨於此。從家族史中,發展出各種不同的計分方式,主要是計算家族成員中得到乳癌與卵巢癌的個數與發病年齡,有些還合併病理組織學型態計分(如三陰性乳癌之於BRCA1),舉例如modified Manchester score、BRCAPRO score與Myriad score等。
參考過去本院與國外的研究,具有下列早發或是家族史的病友,我們會建議病友在乳癌專科醫師的診治之下,至基因醫學部接受癌症遺傳諮詢,清楚的了解家族性乳癌的資訊後,決定是否進行基因檢驗:
- 您是早發性乳癌(<35歲)或是雙側乳癌的患者。
- 您有≥3名女性家族成員被診斷患有乳癌(年齡:不限制)。
- ≥2的女性家族成員診斷出患有乳腺癌,其中一人被診斷時≤50歲。
- ≥1女性家族成員確診乳癌和一個家族成員確診為卵巢癌(可以是同一位家族成員)
- ≥1女家族成員<35歲確診乳癌。
- ≥1名女性家族成員確診為雙側乳癌(第一個乳癌確診時需<50歲)。
- ≥1名女性家族成員確診為卵巢癌(確診時需<40歲)。
- ≥2名女性家族成員確診為卵巢癌(年齡:不限制)。
- ≥1男性家族成員確診為乳癌(年齡:不限制)。
國外資料於高風險族群,如猶太人或是其他BRCA帶因者,有大規模長期追蹤資料。簡述如下,其預防癌症方式,包含預防性雙側乳房切除、卵巢切除、影像學追蹤(位切除者),化學藥物預防等方法,對照分析為切除或追蹤者。
在該研究中,40歲時預防性卵巢切除可使BRCA1帶因者增加15%絕對存活率;40歲時預防性雙側乳房切除可使BRCA2帶因者增加7%絕對存活率。若是乳房與卵巢都切除,可使BRCA1帶因者增加24%絕對存活率,BRCA2帶因者增加11%絕對存活率[16,17](圖1)。但是器官切除對身心影響,也是必須考慮的重要因素,文中指出,定其影像學追蹤(mammography plus MRI),也可以是一個合理的選擇。而另一個大規模研究也顯示,帶因者定期接受mammography與MRI追蹤,可以有效降低晚期乳癌的發生率。
至於化學性預防是使用自然或合成藥物來減低癌的擴散或防止再得到癌的機會。例如:一項美國國家級的乳癌研究 NSABP P-1 trial (National Surgical Adjuvant Breast and Bowel Project Breast Cancer Prevention trial ),發現常用的乳癌抗賀爾蒙藥物Tamoxifen能減低62% BRCA2乳癌的發生案例,不過,Tamoxifen的使用對BRCA1的女性並無明顯預防作用[19],至於其它的化學預防還有待觀察。為何Tamoxifen僅對BRCA2基因突變的病人有預防保護的效果,可能原因就如前段所述,因BRCA2基因突變發生的乳癌大多為賀爾蒙接受體陽性,BRCA1基因突變者產生的多為三陰性乳癌,因此對於抗賀爾蒙藥物自然無效。
就目前的研究資料顯示,化學性預防的效果仍不如預防性手術。目前僅被當作是高風險婦女,又不願意或無法接受預防性切除手術的替代選擇 (主要是使用Tamoxifen)。
林柏翰醫師